制剂开发
- 选择
- 选择
Formulation Development, Early Phase
我们的口服固体制剂开发团队在加快推动候选药物从临床前到临床以及到商业化生产方面有着丰富的经验。
我们成功应对了生物利用度差、辅料不兼容、载体稳定性和最佳释放曲线等的各种挑战。我们现在为全球市场的 10 多种商业化药物制剂提供支持。
我们的服务范围覆盖了各种各样的口服剂型,并建立了一个包括喷雾干燥分散体、热熔挤出、纳米研磨和脂质制剂在内的全面的赋能技术平台。
我们还提供口服高活药物的制剂开发和生产服务,其职业接触限值(OEL)低至 10 ng/m3。
速度
- 制剂开发最快需要 1-6 周
- 从 GMP 原料药的接收到 1 期临床样品的放行最快需要 4-6 周( F2CS 服务)
- 从技术转移到 PPQ 放行最快需要 6 个月 (F4CL 服务)
经验
- 在 2024 年支持了超过 1,000 个分子(从临床前期到3期临床)
- 在 2024 年生产了超过 2,600 批次
- 迄今为止支持了 14 个药品成功商业化
Speed
- 4-6 weeks from GMP API received to phase I CTM released (F2CS)
- 1-6 weeks for formulation development
Experience
- 2,500+ compounds assessed annually
- 300+ formulations developed annually
用于1期临床试验的一体化服务( F2CS 服务)
为快速交付 I 期临床试验所需样品而设计的制剂一体化服务
您的创新疗法已到了关键的里程碑——IND 申报。当日期迅速临近时,您需要一个可靠的合作伙伴来开发和生产您的制剂,以满足申报要求和 I 期临床研究的用药需求。
每一项创新都是独一无二的,因此您需要合适的制剂和剂型选择,并快速使用模型来确定最佳选项——而不是一概而论的思路。
合全药业的 F2CS 服务将我们的能力、专业知识和先进技术应用于快速交付您的临床试验样品。我们承诺在 8 周内完成制剂开发和临床试验样品的供应。

为什么信赖 F2CS 服务?
合全药业的团队经验丰富,在 2024 年支持了超过 1,000 种临床前到 III 期的不同剂型的分子。我们的团队利用各种剂型,包括全面的生物利用度增强工具,快速开发最佳的制剂来快速交付临床试验样品。
快速 – 我们的原料药、制剂、分析和全球药学事务申报的支持团队并行工作,节省时间并快速完成您的项目。我们庞大的团队和产能能够快速适应意外的情况,确保按时交付,并且控制在预算内。
灵活 – 我们的团队在各种剂型方面拥有丰富的经验,并配备了多种工艺方法。他们能够使用最先进的生物利用率增强技术,选择和设计最佳的剂型,以实现最佳的药物暴露。
一体化 – 制剂和分析团队位于距离原料药团队 2 小时车程的地点,使得协作、问题解决、调度和物料转移快捷方便。
生物利用度增强技术
- 喷雾干燥
- 热熔挤出
- 纳米研磨
- 脂质制剂
灵活的制剂及工艺选项
- 原料药置于瓶中或者胶囊里
- 胶囊内的粉末
- 片剂
- 脂质制剂
- 干法制粒
- 直接压片
- 湿法制粒
一体化CMC服务
- 原料药工艺研发和生产
- 分析开发及验证
- 稳定性测试
- 包装和贴标
- CMC材料写作
- 经过验证的质量,环境、健康、安全(EHS)系统
Fast to Clinical Supply
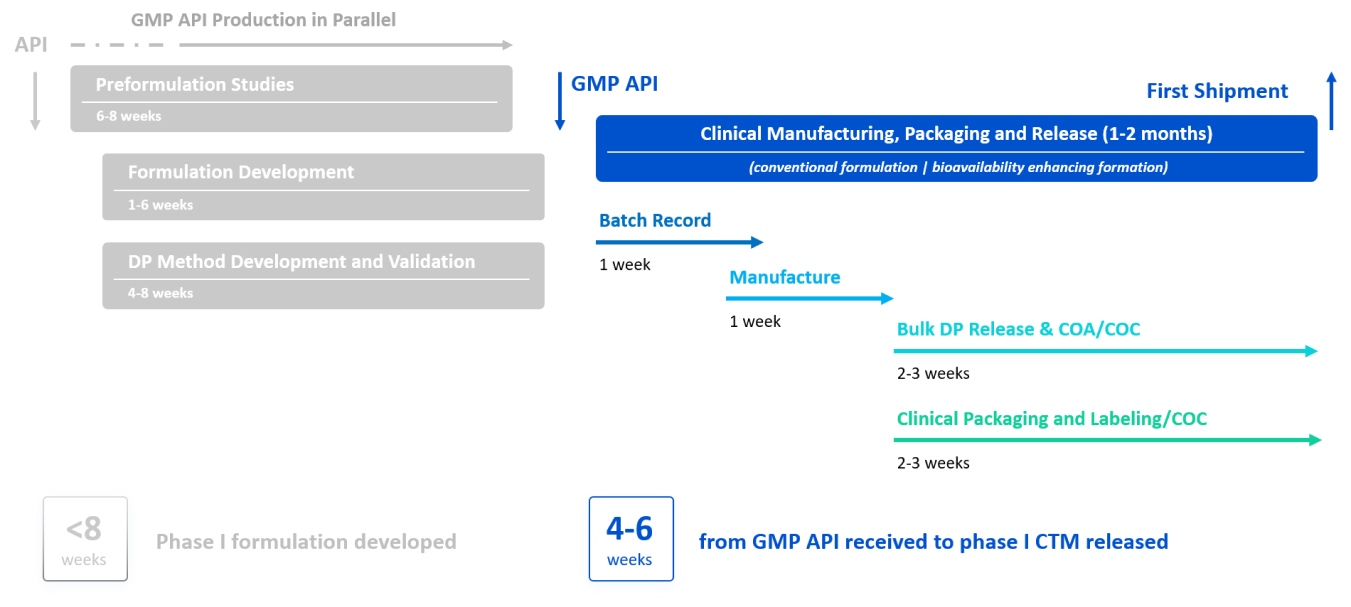
Speed
- Technology transfer to release of PPQ completed in 6 months (F4CL)
Experience
- 500+ molecules in Phase II and beyond (2022)
- 2,800+ clinical and commercial batches manufactured (2022)
- 8 commercial projects
用于上市的一体化服务( F4CL 服务)
为全球市场快速上市设计的制剂一体化服务
当您的 CMC 项目接近最后一步,即 NDA 申报时,您需要考虑如何确保您的药物成功进入目标的市场。
各个国家的监管机构有不同的要求和时间表。与正确的合作伙伴一起工作,您就不需要担心您不熟悉的市场。合全药业在全球申报的所有 CMC 活动和项目规划上都有丰富的经验。
我们专门的一体化服务——Fast for Commercial Launch(F4CL),可以支持您在全球范围内同步上市药物,并且确保速度、可靠性和质量。

为什么信赖 F4CL 服务?
合全药业在北美、欧洲和亚洲拥有大量的制剂和分析研究员的团队,支持您全球上市目标的设计和实施。
速度
我们一体化原料药和制剂的 CMC 平台拥有庞大的团队,既可以提供高产量,也能保证灵活性,尽可能地定制您的计划并平行运行项目,以缩短提交时间。
能力
我们的制剂团队拥有全面的剂型开发能力(包括口服和注射剂型),配备商业化规模赋能技术(包括喷雾干燥和热熔挤出)的先进设施,以更好地支持您所选的剂型。
经验
我们一体化团队拥有丰富的经验和专有技术,推进后期 CMC 项目交付,已支持了 14 个商业化药物。
可靠性
我们一体化 CMC 平台目前已支持 1,000 多种新药分子。在全球范围内,我们近年来支持了 50 多种新药通过审批,在 105 个以上国家上市。
质量
每个基地均由一致的质量体系所管理,全球主要监管机构的审查和每年数百次的客户审计证明我们质量体系的完善。
Formulation Development, Late Phase
Our dedicated late phase teams have rich experience in pushing your candidates from early stage to pivotal clinical, process optimization via DoE, process validation, and NDA registration, until commercialization.
We have supported validation of 20+ NCEs since 2019 with 100% PPQ success, and have successfully enabled 7 drug product approvals for the global market. Our GMP facilities in Shanghai, Wuxi city, China and Couvet, Switzerland have been inspected by the US FDA, EMA, China NMPA, Japan PMDA, SwissMedic and many other regulatory agencies, equipped with advanced commercial equipment for spray dried dispersion, hot melt extrusion, dry/wet/fluid bed granulation, continuous manufacturing, high potency drug product and many more.